
Mit Klick in einer Zeile auf 'Nummer' oder 'Titel' erhält man in einem Kasten weitere Einzelheiten!
1. der Konzentration
2. der Ladungsgröße und
3. der Beweglichkeit der Ionen.
Experiment Multiadapter TH Experiment Video AK 32 Teachers Helper Aufgaben Lowcost Leitfaehigkeit Multiadapter Selbstbau
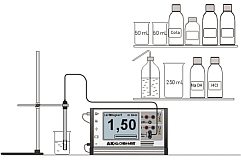
Experiment Multiadapter TH AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Strom Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Lowcost Leitfaehigkeit Multiadapter TH

Experiment AK Analytik 11 All Chem Misst Lowcost Potential Multiadapter
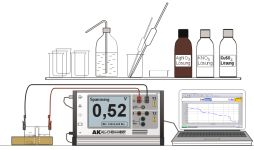
Experiment AK 32 All Chem Misst Lowcost Potential Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Potential Multiadapter
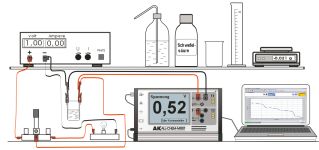
Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Potential Teachers Helper Multiadapter TH

Experiment Lowcost Potential Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Potential Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Potential Teachers Helper Multiadapter TH

Experiment Experiment Video All Chem Misst Ohne Rechner Lowcost Potential Teachers Helper Aufgaben Multiadapter TH

(Achtung: die abgebildete Cola-Dose ist aus Weißblech!)
Als Elektrolyt kann Salzwasser dienen.
Experiment Experiment Video All Chem Misst Ohne Rechner Lowcost Potential Teachers Helper Aufgaben Multiadapter TH

Besonderheit: Die lästige, aber bei pH-Elektroden notwendige Kalibrierung ist ganz einfach, weil jeder Schritt auf dem Touchscreen vorgegeben wird.
Experiment AK Analytik 11 AK 32 THeorie All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Aufgaben Multiadapter

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Ph Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH
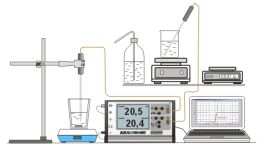
Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Aufgaben Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Aufgaben Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH
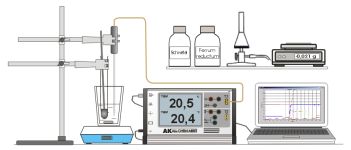
Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 Lowcost Medizintechnik All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH
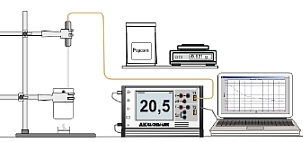
Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment Experiment Video AK Analytik 11 AK 32 Lowcost Medizintechnik All Chem Misst Teachers Helper Aufgaben Multiadapter TH Selbstbau
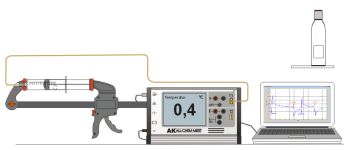
Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Aufgaben Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Multiadapter TH

Experiment AK Analytik 11 AK 32 All Chem Misst Lowcost Temperatur Teachers Helper Aufgaben Multiadapter TH
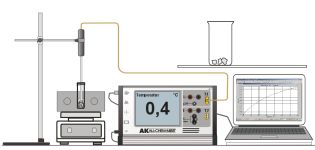
Wiederholung des Versuches mit Papier und Holz.
Experiment Experiment Video AK Analytik 11 AK 32 All Chem Misst Teachers Helper Aufgaben Multiadapter TH
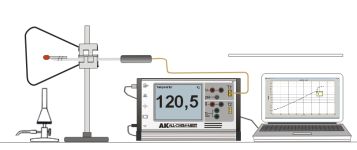
Experiment Experiment Video AK Analytik 11 Lowcost Medizintechnik Teachers Helper Strom Aufgaben Multiadapter Selbstbau Selbstbau Video

Experiment AK Analytik 11 Teachers Helper Strom Multiadapter
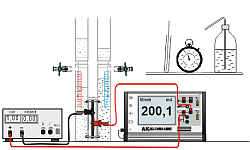
Experiment AK Analytik 11 Teachers Helper Strom Multiadapter

Experiment AK Analytik 11 Teachers Helper Strom Multiadapter
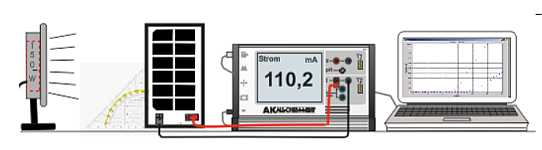
Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Multiadapter
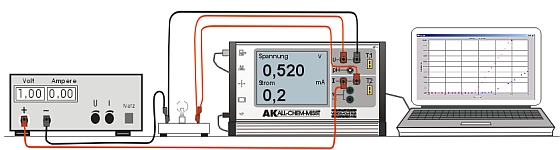
Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
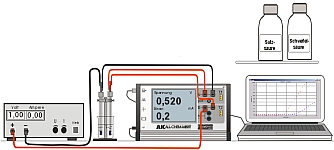
Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Multiadapter

Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
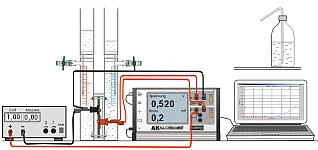
Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
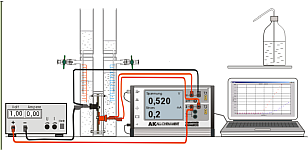
Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
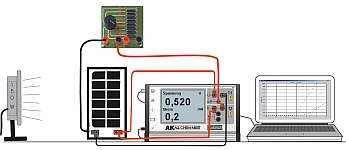
Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
Experiment AK Analytik 11 AK 32 All Chem Misst Teachers Helper Multiadapter

Experiment AK Analytik 11 All Chem Misst Teachers Helper Multiadapter
